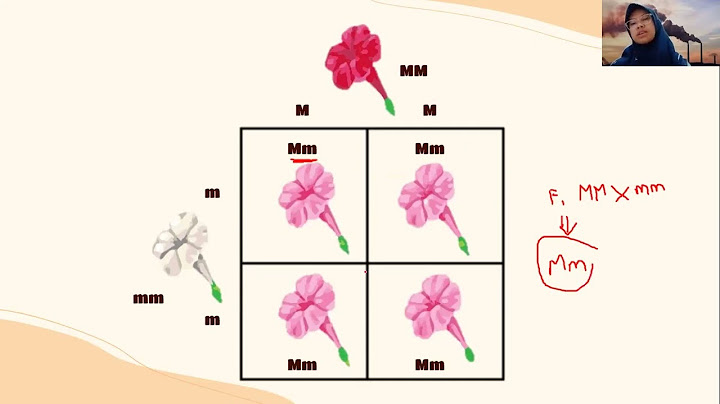
Sistem periodik unsur adalah susunan unsur-unsur berdasarkan urutan nomor atom dan kemiripan sifat unsur-unsur tersebut. Disebut “periodik”, sebagaimana terdapat pola kemiripan sifat unsur dalam susunan tersebut. Sistem periodik unsur (tabel periodik) modern yang saat ini digunakan didasarkan pada tabel yang dipublikasikan oleh Dmitri Mendeleev pada tahun 1869. Show Lihat juga materi StudioBelajar.com lainnya: Tabel Sistem Periodik Unsur (Sumber: Silberberg, Martin S. 2009. Chemistry: The Molecular Nature of Matter and Change (5th edition). New York: McGraw Hill) Format tabel periodik:
Sifat-sifat pada sistem periodik unsur:Sifat logamBerdasarkan sifat, unsur-unsur dapat dikelompokkan menjadi logam, nonlogam, dan metalloid. Unsur-unsur logam memiliki sifat-sifat: konduktor panas dan listrik yang baik, dapat ditempa dan ductile, titik leleh relatif tinggi, cenderung melepaskan elektron kepada unsur nonlogam. Unsur-unsur nonlogam memiliki sifat-sifat: nonkonduktor panas dan listrik, tidak dapat ditempa dan rapuh/getas, kebanyakan berwujud gas pada temperatur kamar, cenderung menerima elektron dari unsur logam. Unsur-unsur metalloid memiliki sifat-sifat seperti logam dan juga nonlogam. Sifat logam semakin berkurang dari kiri ke kanan dan dari bawah ke atas sistem periodik unsur, kecuali hidrogen. Unsur-unsur metalloid berada pada “tangga” yang membatasi unsur-unsur logam dan nonlogam. Jari-jari atomJari-jari atom adalah setengah dari jarak antara dua inti dari dua atom logam yang sejajar atau dalam sebuah molekul diatomik. Dalam satu golongan, dari atas ke bawah, jari-jari atom cenderung semakin besar, sebagaimana pertambahan kulit elektron. Dalam satu periode, dari kiri ke kanan, jari-jari atom cenderung semakin kecil, sebagaimana pertambahan muatan inti efektif. Energi ionisasiEnergi ionisasi adalah energi yang dibutuhkan oleh sebuah atom atau ion dalam fase gas untuk melepaskan sebuah elektronnya. Dalam satu golongan, dari atas ke bawah, energi ionisasi pertama cenderung semakin kecil, sebagaimana jarak dari inti ke elektron terluar bertambah sehingga tarikan elektron terluar oleh inti berkurang. Dalam satu periode, dari kiri ke kanan, energi ionisasi pertama cenderung semakin besar, sebagaimana pertambahan muatan inti efektif sehingga tarikan oleh inti bertambah.  (Sumber: Petrucci, Ralph H. et al. 2011. General Chemistry: Principles and Modern Applications (10th edition). Toronto: Pearson Canada Inc.) Jari-jari ionJari-jari ion adalah jari-jari dari kation atau anion yang dihitung berdasarkan jarak antara dua inti kation dan anion dalam kristal ionik. Kation (ion bermuatan positif) terbentuk dari pelepasan elektron dari kulit terluar atom netral sehingga tolakan antar elektron berkurang, tarikan elektron oleh inti lebih kuat, dan jari-jari dari kation lebih kecil dari atom netralnya. Anion (ion bermuatan negatif) terbentuk dari penangkapan elektron pada atom netral sehingga tolakan antar elektron bertambah dan jari-jari dari anion lebih besar dari atom netralnya. Dalam satu golongan pada sistem periodik unsur, dari atas ke bawah, jari-jari ion bermuatan sama cenderung semakin besar, sebagaimana pertambahan kulit elektron. Dalam periode, pada deretan ion isoelektronik (spesi-spesi dengan jumlah elektron sama dan konfigurasi elektron sama, seperti O2-, F–, Na+, Mg2+, dan Al3+ dengan 10 elektron), semakin besar muatan kation maka semakin kecil jari-jari ion, namun semakin besar muatan anion maka semakin besar jari-jari ion.  (Sumber: Silberberg, Martin S. 2009. Chemistry: The Molecular Nature of Matter and Change (5th edition). New York: McGraw Hill) Afinitas elektronAfinitas elektron adalah kuantitas perubahan energi ketika sebuah atom atau ion dalam fase gas menerima sebuah elektron. Jika kuantitas perubahan energi bertanda positif, terjadi penyerapan energi, sedangkan jika bertanda negatif, terjadi pelepasan energi. Semakin negatif nilai afinitas elektron, semakin besar kecenderungan atom atau ion menerima elektron (afinitas terhadap elektron semakin besar). Dalam satu golongan pada tabel periodik unsur, dari atas ke bawah, afinitas elektron cenderung semakin kecil, dengan banyak pengecualian. Dalam satu periode, dari kiri ke kanan, sampai golongan 7A, afinitas elektron cenderung semakin besar, dengan banyak pengecualian.
  (Sumber: Gilbert, Thomas N. et al. 2012. Chemistry: The Science in Context (3rd edition). New York: W. W. Norton & Company, Inc.) ElektronegativitasElektronegativitas adalah ukuran kemampuan suatu atom dalam sebuah molekul (keadaan berikatan) untuk menarik elektron kepadanya. Semakin besar elektronegativitas, semakin mudah atom tersebut menarik elektron kepadanya sendiri. Dalam satu golongan, dari atas ke bawah, elektronegativitas cenderung semakin kecil. Dalam satu periode, dari kiri ke kanan, elektronegativitas cenderung semakin besar.  (Sumber: Petrucci, Ralph H. et al. 2011. General Chemistry: Principles and Modern Applications (10th edition). Toronto: Pearson Canada Inc.) Sistem Periodik Unsur – Referensi – Silberberg, Martin S. 2009. Chemistry: The Molecular Nature of Matter and Change (5th edition). New York: McGraw Hill – Stacy, Angelica M. 2015. Living by Chemistry (2nd edition). New York: W.H. Freeman and Company – Tro, Nivaldo J. 2011. Introductory Chemistry (4th edition). Illinois: Pearson Prentice Hall. Judul Artikel: Sistem Periodik Unsur Kontributor: Nirwan Susianto, S.Si. Alumni Kimia UI Materi StudioBelajar.com lainnya:
Merdeka.com - Setiap jenis atom yang ada di dunia tentu punya panjang jari-jari yang berbeda. Lalu, tahukah kamu apa yang mempengaruhi perbedaan panjang jari-jari atom? Sebelumnya, pahami dulu definisi jari-jari atom. Jari-jari atom (R) merupakan jarak dari pusat atom (inti atom) sampai kulit elektron terluar yang ditempati elektron. Panjang pendeknya jari-jari atom ditentukan oeh 2 faktor yaitu: 1. Jumlah kulit atom Makin banyak jumlah kulit yang dimiliki suatu atom, maka otomatis jari-jari atomnya juga makin panjang. Jari-jari atom Natrium lebih panjang daripada jari-jari atom Litium, karena jumlah kulit yang dimiliki atom Natrium lebih banyak daripada atom Litium. 2. Muatan inti atom Bila jumlah kulit dari dua atom sama banyak, maka yang berpengaruh terhadap panjangnya jari-jari atom adalah muatan inti atom. Makin banyak inti atom berarti makin besar muatan intinya dan gaya tarik inti atom terhadap elektron lebih kuat sehingga elektron lebih mendekat ke inti atom. Dalam tabel periodik bisa diamati bahwa:
|

Pos Terkait
Periklanan
BERITA TERKINI
Toplist Popular
#1
#2
#4
#5
#6
#7
Top 8 apa itu benedict dan biuret? 2022
1 years ago#8
#9
#10
Top 6 apa itu self pick up grabfood? 2022
2 years agoPeriklanan
Terpopuler
Periklanan
Tentang Kami
Dukungan

Copyright © 2024 toptenid.com Inc.